【產(chǎn)品名稱】
通用名:呼吸道六種病毒核酸檢測試劑盒(熒光 PCR 法)
【包裝規(guī)格】
貨號:A65324
規(guī)格:50 人份/盒�����。
【預(yù)期用途】
呼吸道腺病毒(Radv)����、人偏肺病毒(HMPV)�、人鼻病毒(HRV)、
呼吸道合胞病毒(RSV)核酸的定性檢測����,用于呼吸道副流感
病毒Ⅰ/Ⅲ型(PIVⅠ/Ⅲ)、呼吸道腺病毒(Radv)��、人偏肺病毒
(HMPV)����、人鼻病毒(HRV)、呼吸道合胞病毒(RSV)感染
的輔助診斷及流行病學(xué)監(jiān)控���。
【檢測原理】
本試劑盒根據(jù)熒光 PCR 技術(shù)原理���,針對呼吸道副流感病
毒Ⅰ/Ⅲ型(PIVⅠ/Ⅲ)���、呼吸道腺病毒(Radv)、人偏肺病毒
(HMPV)�����、人鼻病毒(HRV)��、呼吸道合胞病毒(RSV)設(shè)計(jì)
特異性引物和 Taqman 探針����,通過熒光定量 PCR 儀進(jìn)行擴(kuò)增,
從而實(shí)現(xiàn)對呼吸道副流感病毒Ⅰ/Ⅲ型(PIVⅠ/Ⅲ)�、呼吸道腺
病毒(Radv)、人偏肺病毒(HMPV)���、人鼻病毒(HRV)����、呼
吸道合胞病毒(RSV)核酸的檢測�。
【主要組成成分】
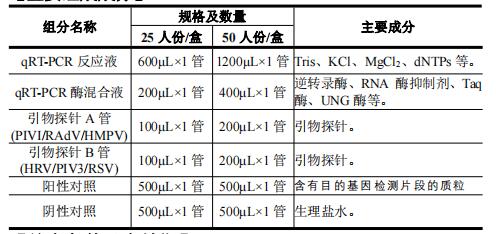
【儲(chǔ)存條件及有效期】
1.避光-20±5℃儲(chǔ)存,有效期 12 個(gè)月����。
2.采用泡沫箱加冰袋的運(yùn)輸方式�,運(yùn)輸不超過 4 天��;開封
后避光-20±5℃儲(chǔ)存����;反復(fù)凍融不超過 6 次。
3.生產(chǎn)日期�、有效期至:見外包裝盒。
【適用儀器】
適 用 于 ABI 7500 ���、 Bio-Rad CFX96 、 Roche
Lightcycler480I�、Lightcycler480II、cobas Z480����、宏
石 SLAN-96S、SLAN-96P 等實(shí)時(shí)熒光定量 PCR 儀��。
【樣本要求】
1.樣本類型:上呼吸道標(biāo)本(包括咽拭子����、鼻拭子����、鼻咽
抽取物���、深咳痰液)���;下呼吸道標(biāo)本(包括呼吸道抽取
物、支氣管灌洗液����、肺泡灌洗液、肺組織活檢標(biāo)本)�����;
組織培養(yǎng)物等樣品��。
2.保存條件:采集的樣本應(yīng)及時(shí)送檢��,24 小時(shí)內(nèi)檢測的
應(yīng) 4℃保存����,超過 24 小時(shí)的-70℃保存(如無-70℃保存
條件,待測樣本可于-20℃冰箱保存 10 天)�,并避免反
復(fù)凍融���。
【檢測方法】
1.試劑準(zhǔn)備(試劑準(zhǔn)備區(qū))
將試劑盒各組分室溫融化,充分振蕩混勻后瞬時(shí)離心��。
計(jì)算試劑使用份數(shù) N(N=樣本數(shù)+1<陽性對照>+1<陰性對
照>)����,根據(jù)下表配置反應(yīng)體系,將各組分加入至同一適當(dāng)
體積離心管中�����,充分混勻后瞬時(shí)離心����,配制成反應(yīng)體系混
合液�,按 20μL/孔分裝至 PCR 反應(yīng)管/板,并轉(zhuǎn)移至樣本處
理區(qū)�。

2.樣本處理(樣本處理區(qū))
① 核酸提取
選擇合適的核酸提取試劑盒提取樣本核酸,具體按照
相應(yīng)的試劑盒說明書操作����。
② 加樣
在已加入反應(yīng)體系混合液的 PCR 反應(yīng)管/板上分別加
入處理好的待檢樣本核酸、陰性對照�、陽性對照各 5μL���,
終體積為 25μL。蓋緊管蓋或封膜��,瞬時(shí)離心后置熒光 PCR
擴(kuò)增儀上檢測�。
3.?dāng)U增檢測(核酸擴(kuò)增區(qū))
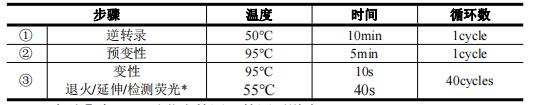
*步驟③中 55℃時(shí)熒光檢測,檢測通道為 FAM��、VIC/HEX��、CY5���。
*ABI 系列熒光 PCR 儀不選 ROX 校正�����,淬滅基團(tuán)選 None���。
4.結(jié)果分析
根據(jù)分析后圖像調(diào)節(jié)起止值,(建議起始設(shè)在 3~15�����、
終止設(shè)在 5~20,同時(shí)調(diào)整陰性對照的擴(kuò)增曲線平直或低于
閾值線)��,點(diǎn)擊分析�����,在報(bào)告界面查看結(jié)果����。
【質(zhì)量控制】
1.陰性對照:Ct 值>38 或未檢出。
2.陽性對照:擴(kuò)增曲線呈典型 S 型����,且 Ct 值≤35。
3.同一實(shí)驗(yàn)以上要求需同時(shí)滿足�,否則本次實(shí)驗(yàn)視為無效。
【結(jié)果判讀】
①陽性判讀:
A 管陽性判讀:
a:FAM 通道 Ct≤35���,副流感 I 型病毒陽性�����;
b:VIC 通道 Ct≤35,呼吸道腺病毒陽性�;
c:CY5 通道 Ct≤35,人偏肺病毒陽性;
B 管陽性判讀:
a:FAM 通道 Ct≤35�,人鼻病毒陽性;
b:VIC 通道 Ct≤35����,副流感病毒Ⅲ型陽性;
c:CY5 通道 Ct≤35����,呼吸道合胞病毒陽性;
②陰性判讀:FAM 通道或 VIC 通道或 CY5 通道 Ct 值>38
或未檢出��,判為陰性�。
③復(fù)測:
FAM 通道或 VIC 通道或 CY5 通道 35<Ct 值≤38,
需復(fù)檢��;復(fù)檢結(jié)果若一致��,判定結(jié)果為陽性��。
【檢驗(yàn)方法的局限性】
1. 樣品采集�、運(yùn)輸、保存不當(dāng)�����,試劑運(yùn)輸、保存�����、配制不當(dāng)都可
能會(huì)影響實(shí)驗(yàn)結(jié)果�����,甚至?xí)?dǎo)致假陰性結(jié)果����。
2. 如果實(shí)驗(yàn)室污染、試劑污染���、樣品交叉污染��,可能出現(xiàn)假陽性
結(jié)果�����。
【試劑盒性能指標(biāo)】
1. 最低檢測限:500copies/mL���。
2. 特異性:針對可能與檢測靶標(biāo)產(chǎn)生交叉的其他病原無交叉反應(yīng)。
【注意事項(xiàng)】
1. PCR 操作各階段應(yīng)嚴(yán)格分區(qū)操作�,避免交叉污染。
2. 試劑盒各組分使用前應(yīng)充分融化混勻�,離心數(shù)秒后使用。
3. 各組分不得與其他產(chǎn)品或不同批號的相應(yīng)成分進(jìn)行互換��。
4. 待測標(biāo)本若不及時(shí)檢測���,應(yīng)保存于-70℃�����。
5. 樣品的處理應(yīng)該嚴(yán)格按照生物安全規(guī)范操作�����。
6. PCR 操作人員應(yīng)具有經(jīng)驗(yàn)和受過專業(yè)培訓(xùn)���。
7. 本試劑盒僅用于科研使用,不做為臨床診斷使用�����。